|
mRNA 疫苗研發好幫手:TransIT®-mRNA 轉染試劑 (Mirus Bio)
|
美國莫德納藥廠、法國賽諾菲巴斯德藥廠、中國科學院……在 mRNA 疫苗開發初期「in vitro RNA expression」實驗階段的共同選擇:TransIT®-mRNA Transfection Kit
|
 自 2019 年 12 月新冠肺炎 (COVID-19) 爆發以來,疫情迅速擴散造成全球大流行,不僅嚴重威脅人類生命健康也為疫苗與製藥產業帶來極大挑戰!《Nature》期刊於 2020 年 8 月 5 日詳盡報導了由莫德納藥廠 (Moderna Inc.)、美國國家過敏和傳染病研究所 (NIAID)、北卡羅來納大學教堂山分校、喬治華盛頓大學、范登堡大學附設醫學中心、德州大學奧斯汀分校等 62 人所組成的超級任務團隊,如何在新型冠狀病毒 (SARS-CoV-2) 基因體序列公佈後的第 3 天迅速完成莫德納新冠肺炎疫苗 (mRNA-1273) 的序列設計,更創紀錄地在第 66 天(2020 年 3 月 16 日)即進入第一期臨床試驗 [1],第三期臨床試驗結果也已在 2020 年底公佈 [2, 3]。 自 2019 年 12 月新冠肺炎 (COVID-19) 爆發以來,疫情迅速擴散造成全球大流行,不僅嚴重威脅人類生命健康也為疫苗與製藥產業帶來極大挑戰!《Nature》期刊於 2020 年 8 月 5 日詳盡報導了由莫德納藥廠 (Moderna Inc.)、美國國家過敏和傳染病研究所 (NIAID)、北卡羅來納大學教堂山分校、喬治華盛頓大學、范登堡大學附設醫學中心、德州大學奧斯汀分校等 62 人所組成的超級任務團隊,如何在新型冠狀病毒 (SARS-CoV-2) 基因體序列公佈後的第 3 天迅速完成莫德納新冠肺炎疫苗 (mRNA-1273) 的序列設計,更創紀錄地在第 66 天(2020 年 3 月 16 日)即進入第一期臨床試驗 [1],第三期臨床試驗結果也已在 2020 年底公佈 [2, 3]。
另一方面,中國疾病預防控制中心 (CDC) 與中國科學院正通力合作,期望開發出僅需要施打一劑就能達到長期保護效果的新冠肺炎 mRNA 疫苗 [4]。如同莫德納疫苗,中國 CDC 與中國科學院團隊同樣在疫苗研發初期 in vitro RNA expression 實驗階段,選擇使用美國 Mirus Bio 公司所開發的 mRNA 轉染試劑「TransIT®-mRNA Transfection Kit」來進行 mRNA 疫苗的細胞轉染實驗,以確認 mRNA 疫苗能夠在細胞中正常表達出目標蛋白質 [1, 4]。其他諸如美國賓州大學醫學院 [5]、法國賽諾菲巴斯德藥廠 (Sanofi Pasteur) [6] 等知名新冠肺炎 mRNA 疫苗研發單位,也同樣選擇使用 TransIT-mRNA 轉染試劑。另一個知名的 mRNA 醫藥研發公司——德國 BioNTech ——則是在其一篇探討如何移除體外轉錄 (in vitro-transcribed, IVT) mRNA 產物的 dsRNA 不純物的文章中,將 TransIT-mRNA 試劑作為 IVT mRNA 產物的包裹物,應用於動物實驗 [7]。
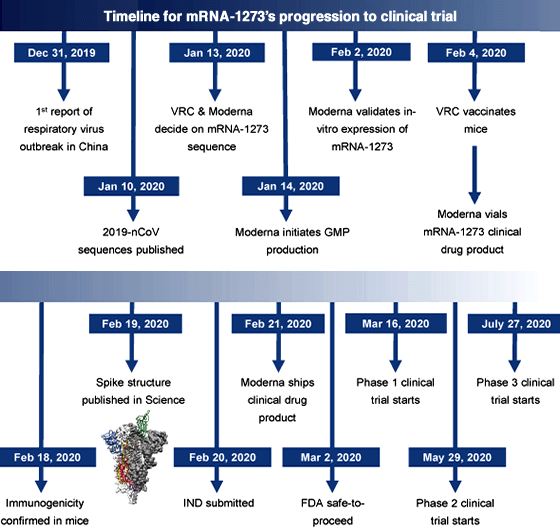
圖 1﹑莫德納新冠肺炎疫苗 (mRNA-1273) 研發時間軸(顯示至第三期臨床試驗啟動)。 © Nature. 2020 Oct;586(7830):567-571. Extended Data Fig. 2 [1].
除了新冠病毒,TransIT-mRNA 轉染試劑也參與了流感病毒 (influenza virus) [8]、愛滋病毒 (HIV-1) [9]、登革熱病毒 (Dengue virus) [10] 以及三陰性乳癌 [11] 的 mRNA 疫苗研究。不難發現,隨著新冠肺炎帶動起的 mRNA 疫苗與 mRNA 藥物熱潮,TransIT-mRNA 幾乎是所有主要核心研究單位的共同選擇,以下我們就透過評比實驗帶您進一步來了解 TransIT-mRNA 的優勢與特性。
|
評比實驗顯示,TransIT®-mRNA Transfection Kit 不僅具有優異的轉染效率,細胞毒性也更低,讓您更容易獲取穩定高再現性的實驗結果
|
Mirus Bio 公司所開發的 TransIT-mRNA 轉染試劑能夠非常有效率地將單個或多個不同長度的 RNA 序列送入細胞,應用領域包含蛋白質表現、病毒顆粒生產、CRISR/Cas9 基因編輯等。在以下評比實驗中,我們測試了 TransIT®-mRNA Transfection Kit (Mirus Bio)、Lipofectamine® RNAiMAX (Life Technologies) 以及 Stemfect™ RNA Transfection Kit (Stemgent) 這三種 RNA 細胞轉染試劑。所選用的 RNA 材料為帶有 5' 端帽與 3' 端 poly(A) 的 EGFP mRNA,轉染對象為 BJ 纖維母細胞 (BJ fibroblasts)。在進行連續 14 天的重複性轉染後,可以發現 TransIT®-mRNA 與 Stemfect™ 的轉染效率較佳(圖 2, 3),結合細胞存活率 (cell viability) 檢測結果,可以發現 TransIT®-mRNA 不僅具有優異的轉染效率,細胞毒性也最低,安全性遠高於其他兩個產品(圖 3)。
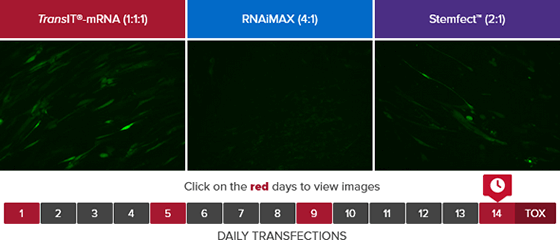
圖 2﹑評比實驗結果 - 細胞螢光影像攝影(點圖看完整短片)
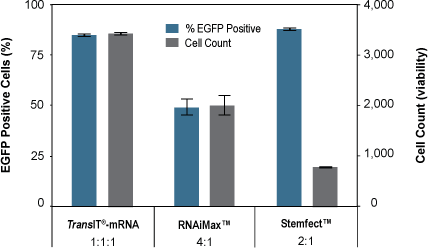
圖 3﹑評比實驗結果 - 轉染效率與細胞存活率(點圖看完整說明)
| Product |
Size |
Cat. No. |
| TransIT®-mRNA Transfection Kit |
1 ml |
MIR2250 |
兼具高轉染效率與低細胞毒性的 TransIT-mRNA 具有十分豐富的文獻紀錄,其中不乏《Cell》《Cell Stem Cell》《Immunity》《Nature》《Neuron》《Science Translational Medicine》等頂尖學術期刊文章。您可以在這個頁面找尋到 TransIT-mRNA 的近期文獻,完整產品資訊、最新活動訊息以及索取試用樣本,歡迎洽詢 Mirus Bio 台灣獨家代理 — 伯森生技(👨💻線上聯絡伯森業務專員)。您可透過下方連結瀏覽更多相關資訊:
References
- Corbett KS, et al. SARS-CoV-2 mRNA vaccine design enabled by prototype pathogen preparedness. Nature. 2020 Oct;586(7830):567-571. PMID: 32756549
- Baden LR, et al. Efficacy and Safety of the mRNA-1273 SARS-CoV-2 Vaccine. N Engl J Med. 2021 Feb 4;384(5):403-416. PMID: 33378609
- Moderna’s Work on our COVID-19 Vaccine. Moderna, Inc. 2021 Oct 26.
- Huang Q, et al. A single-dose mRNA vaccine provides a long-term protection for hACE2 transgenic mice from SARS-CoV-2. Nat Commun. 2021 Feb 3;12(1):776. PMID: 33536425
- Laczkó D, et al. A Single Immunization with Nucleoside-Modified mRNA Vaccines Elicits Strong Cellular and Humoral Immune Responses against SARS-CoV-2 in Mice. Immunity. 2020 Oct 13;53(4):724-732.e7. PMID: 32783919
- Kalnin KV, et al. Immunogenicity and efficacy of mRNA COVID-19 vaccine MRT5500 in preclinical animal models. NPJ Vaccines. 2021 Apr 19;6(1):61. PMID: 33875658
- Baiersdörfer M, et al. A Facile Method for the Removal of dsRNA Contaminant from In Vitro-Transcribed mRNA. Mol Ther Nucleic Acids. 2019 Apr 15;15:26-35. PMID: 30933724
- Freyn AW, et al. Antigen modifications improve nucleoside-modified mRNA-based influenza virus vaccines in mice. Mol Ther Methods Clin Dev. 2021 Jun 12;22:84-95. PMID: 34485597
- Saunders KO, et al. Lipid nanoparticle encapsulated nucleoside-modified mRNA vaccines elicit polyfunctional HIV-1 antibodies comparable to proteins in nonhuman primates. NPJ Vaccines. 2021 Apr 9;6(1):50. PMID: 33837212
- Wollner CJ, et al. A Dengue Virus Serotype 1 mRNA-LNP Vaccine Elicits Protective Immune Responses. J Virol. 2021 May 24;95(12):e02482-20. PMID: 33762420
- Liu L, et al. Combination Immunotherapy of MUC1 mRNA Nano-vaccine and CTLA-4 Blockade Effectively Inhibits Growth of Triple Negative Breast Cancer. Mol Ther. 2018 Jan 3;26(1):45-55. PMID: 29258739
|



 自 2019 年 12 月新冠肺炎 (COVID-19) 爆發以來,疫情迅速擴散造成全球大流行,不僅嚴重威脅人類生命健康也為疫苗與製藥產業帶來極大挑戰!《Nature》期刊於 2020 年 8 月 5 日詳盡報導了由莫德納藥廠 (Moderna Inc.)、美國國家過敏和傳染病研究所 (NIAID)、北卡羅來納大學教堂山分校、喬治華盛頓大學、范登堡大學附設醫學中心、德州大學奧斯汀分校等 62 人所組成的超級任務團隊,如何在新型冠狀病毒 (SARS-CoV-2) 基因體序列公佈後的第 3 天迅速完成莫德納新冠肺炎疫苗 (mRNA-1273) 的序列設計,更創紀錄地在第 66 天(2020 年 3 月 16 日)即進入第一期臨床試驗 [1],第三期臨床試驗結果也已在 2020 年底公佈 [2, 3]。
自 2019 年 12 月新冠肺炎 (COVID-19) 爆發以來,疫情迅速擴散造成全球大流行,不僅嚴重威脅人類生命健康也為疫苗與製藥產業帶來極大挑戰!《Nature》期刊於 2020 年 8 月 5 日詳盡報導了由莫德納藥廠 (Moderna Inc.)、美國國家過敏和傳染病研究所 (NIAID)、北卡羅來納大學教堂山分校、喬治華盛頓大學、范登堡大學附設醫學中心、德州大學奧斯汀分校等 62 人所組成的超級任務團隊,如何在新型冠狀病毒 (SARS-CoV-2) 基因體序列公佈後的第 3 天迅速完成莫德納新冠肺炎疫苗 (mRNA-1273) 的序列設計,更創紀錄地在第 66 天(2020 年 3 月 16 日)即進入第一期臨床試驗 [1],第三期臨床試驗結果也已在 2020 年底公佈 [2, 3]。

