|
看 DELFIA 技術如何助力腫瘤免疫療法研究 — 以標靶單株抗體藥物為例 腫瘤免疫療法 (Immuno-oncology) 在近幾年可說是大放異彩,為癌症治療帶來許多振奮人心的新希望。在本篇文章中,我們將以數個癌症標靶藥物的近期研究為例,帶領大家一同來看 DELFIA 技術如何參與助力標靶單株抗體藥物的開發與改造。 ADCC 簡介 IgG 抗體要發揮功能,除了需要 Fab 區域專一性識別並結合抗原,還需要 Fc 區域來發揮 IgG 的效應功能 (二級功能),例如靶向細胞毒殺等。Fc 區域主要介導以下三類反應: ✅ 抗體依賴性細胞毒殺作用 (Antibody-dependent cell cytotoxicity, ADCC):透過與 NK (Natural killer) 自然殺手細胞表面受體 FcγR (Fcγ receptor) 的結合,協助 NK 細胞辨識標的細胞,並激活 NK 細胞分泌毒性化學物質殺死標的細胞。 ✅ 補體毒殺作用 (Complement dependent cytotoxicity, CDC):透過結合血清補體 C1q,引發一連串的補體活化反應,形成膜攻擊複合體在細胞膜上打洞,最終導致標的細胞膜破裂死亡。 ✅ 延長抗體半衰期:透過與新生兒 Fc 受體 (Neonatal Fc receptor, FcRn) 結合,延長抗體半衰期。
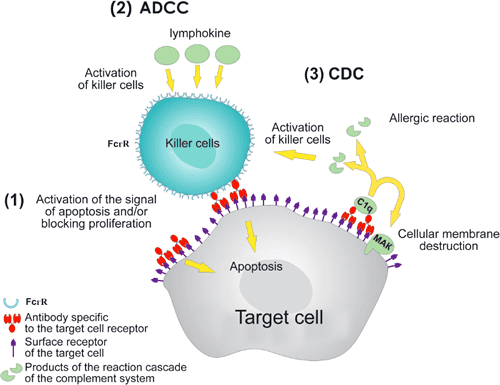
Figure 1. Interaction Pattern of Unloaded Antibodies and Target Cell. (1) Antibodies can cause apoptosis or block the proliferation of target cells, binding with membrane antigens on their surface (membrane raft mechanism). (2) Antibody‑dependent cellular cytotoxicity (ADCC). Killer cells carrying receptors of IgG FcγRI (CD16), FcγRII (CD32), FcγIII (CD64) constant domains (natural killers, killers activated by lymphokines, macrophages, and phagocytes) and receptors of IgE FcεRI and FcεRII (CD23) constant domains (acidocytes) on their surface attack the target cell, whose surface antigens were bound with antibodies. (3) Complement‑dependent cytotoxicity (CDC). Antibodies conjugated in pairs bind to protein С1q complex, causing a cascade of reactions of the complement system, which leads to membrane destruction. Some products of this reaction cascade involve immune cells or cause allergic shock. IMAGE © Acta Naturae. 2009 Apr;1(1):32-50. 基於 DELFIA 技術的 ADCC 檢測 ADCC 本質上屬於免疫細胞媒介產生的細胞毒殺反應,因此常見的針對細胞毒殺 (注意不是細胞存活率或生長速率) 的檢測方式,如經典的 51Cr 釋放法、LDH 檢測、和 Calcein 釋放法等都可以用於 ADCC 檢測。 從原理上,這些方法可區分為「直接法」—— 直接檢測標的細胞在效應免疫細胞作用下的裂解程度,如 51Cr 釋放法;和「間接法」—— 間接檢測效應細胞的活化程度,如 NFAT-RE-luc 報導基因法、和監測剩餘的細胞活力來評估細胞毒殺力,如化學冷光法等。間接法的缺點是不能直接模擬體內 ADCC 過程。 DELFIA® EuTDA 細胞毒殺檢測試劑屬於直接檢測法,更能真實反應臨床抗體藥物引起的 ADCC 作用效果。其偵測原理與 51Cr 釋放法相似,DELFIA® EuTDA 細胞毒殺檢測試劑使用螢光放大配體 BATDA 特異性地標記標的細胞。BATDA 能迅速進入細胞,並在水解作用下形成親水性的 TDA 留在細胞內。當效應免疫細胞裂解標的細胞時,TDA 被釋放至上清液中。當 TDA 和 DELFIA® Eu 試劑相結合時,會形成穩定的強螢光螯合物 EuTDA。藉由偵測最終產物 EuTDA 螢光訊號的強度,可直接反應效應免疫細胞的細胞毒殺能力強弱 [2, 3]。
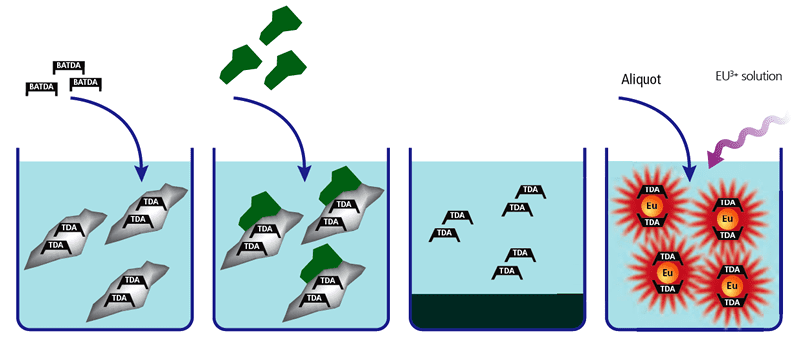
Figure 2. The DELFIA Cytotoxicity assay takes advantage of a fluorescence enhancing ligand (BATDA) which crosses the cell membrane passively, enabling target cell loading that is both rapid and gentle. Once inside the cell, the ligand is immediately hydrolyzed by cellular esterases to generate a hydrophilic molecule (TDA) that can no longer penetrate the membrane. Cytolysis releases TDA into the supernatant to form a highly fluorescent lanthanide chelate with Europium; cytolysis levels are proportional to the amount of fluorescent signal produced. DELFIA® EuTDA 細胞毒殺檢測試劑作為放射性 51Cr 釋放法的取代方法,不僅更為安全且具有眾多優勢。相較於無法區分非特異死亡的 LDH 檢測法,DELFIA® EuTDA 檢測法不受效應免疫細胞死亡和裂解的干擾,降低背景的同時提升了檢測的精確度和穩定性。相較於 Calcein 檢測法,DELFIA® EuTDA 檢測法所採用的 BATDA 能有效標記脆弱細胞,迅速被細胞攝取和在細胞裂解下完成高效的釋放,為 ADCC 檢測提供了穩定的檢測平台和易於標準化等優勢。同時,DELFIA® EuTDA 檢測法不受效應免疫細胞種類限制,靈活支持多種原代免疫細胞 (如 PBMCs (Peripheral blood mononuclear cells) 和 NK 細胞) 和更為穩定的改造細胞系的 ADCC 檢測。 從檢測模式上,DELFIA® EuTDA 採用鑭系元素 (Lanthanide) 中的銪 (Eu) 作為信號源,屬於時差性螢光 (Time-resolved fluorescence, TRF),因此擁有 TRF 本身的眾多優勢,包括不受來源於培養基和血清等的背景螢光干擾,高穩定性和重複性等。此外,Eu 發射光波長落於 615 nm,能有效避免檢測樣本身帶來的干擾,並為多重檢測打下基礎。最後,對自動化和微量化的支持已讓 DELFIA® EuTDA 檢測法逐漸成為大分子藥物研發中 ADCC 檢測的標準方法 [4]。以下我們就來看看幾個採用 DELFIA® EuTDA 進行 ADCC 檢測的臨床標靶藥物研究案例。 標靶單株抗體藥物研發領域之 Fc 區域改造 在談到 Fc 區域改造之前,我們先得進一步了解 ADCC 作用的關鍵成員。在 ADCC 作用中,單株抗體透過其 Fc 區域募集表達有 IgG 受體 FcγR 的免疫細胞 (例如 NK 細胞)。人的 FcγR 包括 FcγRI (CD64,高親和力)、FcγRII (CD32,低親和力)、和 FcγRIII (CD16,低親和力)。Fc 和 FcγR 的結合會引發一系列的免疫活動和多種免疫細胞的活化,達到靶向細胞毒殺的效果。同時,也不是所有的 FcγR 都會激活免疫反應,例如 FcγRIIb 就是一個抑制性 IgG 受體。 早期基於小鼠的研究證明 FcγR 參與了 Rituximab 與 Trastuzumab 的藥效。除此之外亦有多個研究證實,FcγRIIIa 的多型性 (高親和力 - V158;低親和力 - F158) 與單株抗體藥物的臨床治療效果存在有相關性。因此,Fc/FcγR 之間的交互作用是抗體藥效的關鍵調控者,而透過改造 Fc 區域調節其和 FcγR 之間的親和力,也成為單株抗體藥物研發的一個有力切入點。 在此,我們向大家介紹抗體改造的先河研究 [5]。在結構解析的基礎上,該研究引入 AlphaScreen 高通量篩選平台,通過競爭法鑑定出對 FcγRIIIa 具有高親和力的 Fc 區域結構變異體。AlphaScreen 的親和力鑑定結果在 Biacore SPR 檢析中得到了進一步的確認。除了檢測 Fc 區域結構變異體和 FcγRIIIa 之間的親和力,AlphaScreen 還用於確認 Fc 區域結構變異體和抑制性 IgG 受體 FcγRIIb 之間的親和力,從而獲得 Fc 區域結構變異體和 RIIIa/RIIb 的相對親和力比值。以 Trastuzumab 單株抗體為例,實驗結果顯示帶有 S239D/I332E/A330L 三重突變的 Fc 區域結構變異體不僅能提高抗體對激活性受體 FcγRIIIa 的親和力,同時降低了對抑制性受體 FcγRIIb 的親和力,顯著提升 RIIIa/RIIb 的相對親和力比值 (與正常 Trastuzumab 單株抗體相比,比值上升 9 倍)。
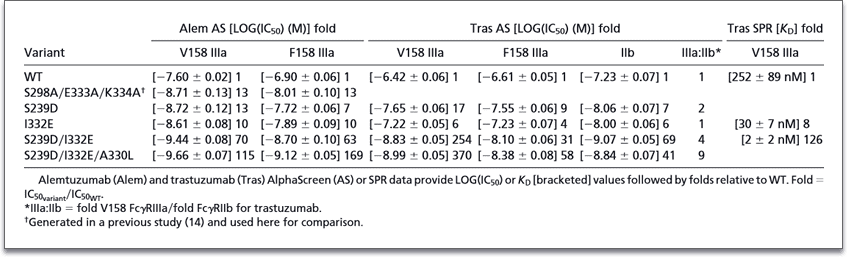
Tabel 1. FcγR affinity enhancements of Fc variants. IMAGE © Proc Natl Acad Sci U S A. 2006 Mar 14;103(11):4005-10. 在親和力篩選的基礎上,作者進一步使用 DELFIA® EuTDA 細胞毒殺檢測試劑驗證 Fc 結構變異體是否的確有助於提升抗體藥物的 ADCC 作用能力。作者以帶有不同 FcγRIIIa 基因型的 PBMCs 作為效應細胞,HER-2 陽性表達的 SkBr3 細胞株作為標的細胞,結果證實帶有 Fc 結構變異體的抗體的確更能有效引發 ADCC 作用,與親和力數據趨勢一致 (下圖左)。而在 HER-2 不同表達程度的細胞株,甚至是幾乎不帶有抗原表達的 MCF7 細胞,均可觀察到 Fc 區域結構變異體更能有效激活 ADCC 作用 (下圖右)。
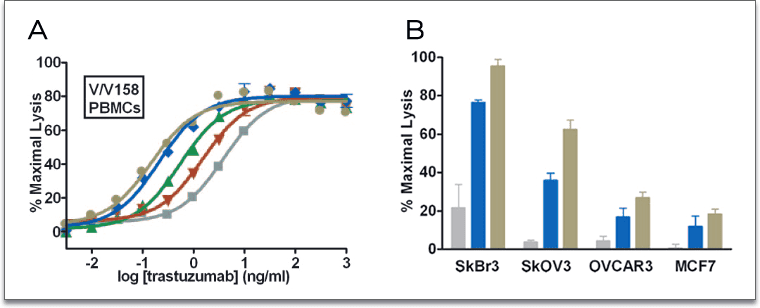
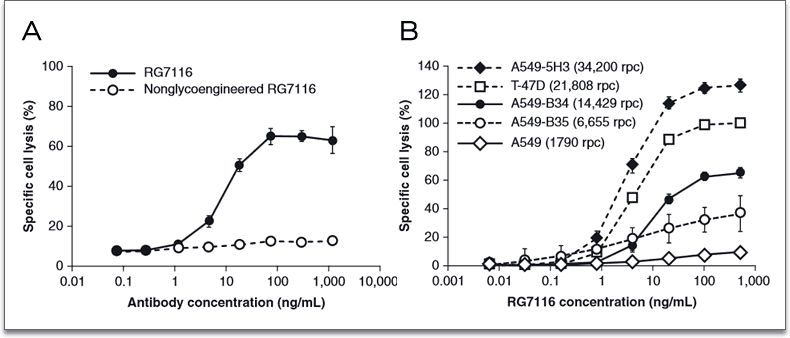
Figure 3. (A) Eu-based detection assays of trastuzumab Abs against SkBr3 breast carcinoma target cells in the presence of human PBMCs allotyped for V/V 158 FcγRIIIa. Gray squares: WT; Green triangles: S239D; Red inverted triangles: I332E; Blue diamonds: S239D/I332E; Tan circles: S239D/I332E/A330L. (B) ADCC of trastuzumab Fc variants against the Her2+ cell lines in the presence of human PBMCs (F/F158 FcγRIIIa). Gray: WT trastuzumab; Blue: S239D/I332E; Tan: S239D/I332E/A330L. IMAGE © Proc Natl Acad Sci U S A. 2006 Mar 14;103(11):4005-10. 除了 Fc 序列變異形成的多型性以外,Fc 區域的醣基化也影響其和 FcγR 的親和力,尤其是岩藻糖 (Fucose) 的缺失會提升 IgG1 和 FcγRIIIa 之間的親和力。因此除了序列突變外,改造 Fc 區域的醣基化修飾也是提升治療性抗體誘發 ADCC 反應的一個途徑。 以羅氏 (Roche) 研發的單株抗體治療藥物 Lumretuzumab (RG7116) 為例 [6],RG7116 一方面可阻斷 HER3 的激活並下調 HER3 的表達,另一方面透過羅氏去岩藻糖修飾的 GlycoMab 技術改造,使 RG7116 和 FcγRIIIa 之間的結合親和力提高 50 倍。而基於 DELFIA 技術的 ADCC 檢測結果也證實,醣基化改造的確能顯著提升 RG7116 的 ADCC 作用活性 (下圖左)。同時,對比不同 HER3 表達量的細胞株,實驗結果清晰顯示 HER3 表達量和 RG7116 介導的 ADCC 作用之間具有正相關性 (下圖右)。 在動物模式上,基於多種低免疫細胞浸潤的小鼠皮下瘤模型,研究發現 RG7116 僅通過靶向 HER3 就能發揮抗癌作用;進一步利用高免疫細胞浸潤的異種原位移植 A549 肺癌小鼠模型,證實醣基化改造的確能有效提升小鼠的生存週期。臨床一期試驗進一步證明 RG7116 的臨床療效。一方面 RG7116 能有效抑制腫瘤細胞膜 HER3 的表達,同時相較於未醣基化改造的 HER3 抗體,RG7116 更能提高 NK 免疫細胞的活化程度 [7]。
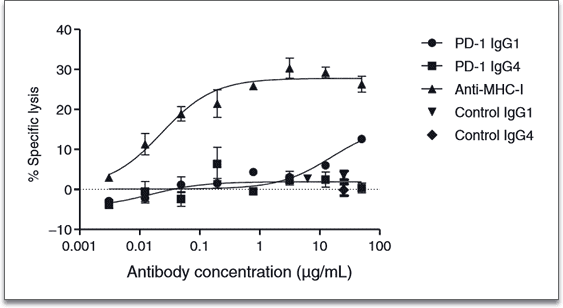
Figure 4. ADCC activity of RG7116 in vitro and in vivo. (A) Glycoengineering of RG7116 resulted in superior in vitro ADCC efficacy compared with nonglycoengineered wild-type RG7116 using recombinant NK92 cells as effectors and T-47D cells as target cells (E:T ratio 5:1). (B) Efficacy of ADCC was associated with HER3 receptor density (E:T ratio 20:1). IMAGE © Cancer Res. 2013 Aug 15;73(16):5183-94. 腫瘤免疫療法領域之首個 PD-1 治療單株抗體:Nivolumab Nivolumab (OPDIVO®) 於 2014 年底獲得美國 FDA 批准用於治療晚期黑色素瘤,成為第一個獲准的 PD-1 抑製劑,標誌著免疫治療時代的開啟。雖然同是單株抗體藥物,PD-1 抑製劑與常見的靶向藥物作用機制不同。PD-1 抗體主要用於阻斷 PD-1 和其配體 PD-L1 的交互作用,而不是殺傷 PD-1 陽性細胞,也就是抗腫瘤效應細胞。在一項關於 Nivolumab 的體外表徵分析研究中,DELFIA® EuTDA 細胞毒殺檢測試劑被用於確認 Nivolumab 是否會誘導 ADCC 產生。作者以活化的 PBMCs 為效應細胞,PD-1 高度表達的 CD4 陽性細胞為標的細胞,結果確認 IgG4 亞型的 Nivolumab 不會誘發 ADCC 效應 [8]。後續的實驗進一步證明 Nivolumab 也不會誘發 CDC 反應,因此 Nivolumab 的引入不會清除 PD-1 陽性細胞群體。
Figure 5. The absence of ADCC by Nivolumab in vitro. IL-2–activated human PBMCs (effector cells) were incubated with activated human CD4+ T cells (target cells) in an effector-to-target cell ratio of 50:1 in the presence of serial dilutions of Nivolumab or a positive control anti-MHC class I antibody for 3 hour at 37°C. IMAGE © Cancer Immunol Res. 2014 Sep;2(9):846-56. 除了 Nivolumab 以外,其他的 PD-1 單株抗體藥物包括 Merck 的 KEYTRUDA®、BeiGene 的 BGB-A317、以及 HengRui 的 SHR-1210,這些都為弱 ADCC 活性設計。然而,同樣是免疫檢查點抑製劑,CTLA-4 單抗 Ipilimumab 則需要其 ADCC 活性來殺傷 Treg 細胞發揮作用,這也說明不同作用機制對治療用抗體誘發 ADCC 反應活性的要求也會有所區別 [9]。 結語 ADCC 活性檢測不僅能協助解析單株抗體藥物的臨床療效,也有助於推動 NK 細胞功能的研究、及開闢新的癌症治療策略。作為成熟的細胞毒殺檢測工具,DELFIA® EuTDA 細胞毒殺檢測試劑不僅可用於評估抗體誘發 ADCC 和 CDC 能力,還能用於檢測 ACT、CAR-T 和 CAR-NK 等療法中免疫細胞的殺傷能力。 針對 ADCC 和 CDC 等細胞毒殺檢測,除了 DELFIA 技術平台,Revvity 還提供黃金標準放射性檢測「51Cr 釋放法」的完善解決方案。詳細產品資訊與應用知識分享,歡迎洽詢 Revvity 台灣代理 — 伯森生技。 References
|

|